 Your new post is loading...
 Your new post is loading...
Arboviruses (arthropod-borne viruses) are a class of viral pathogens that are transmitted by arthropod vectors in nature. They are responsible for many vector-b Ary Faraji, Goudarz Molaei, Theodore G. Andreadis Emerging and lesser-known arboviruses impacting animal and human health
Ary Faraji and others
Journal of Medical Entomology, tjad140, https://doi.org/10.1093/jme/tjad140 Ary Faraji (Data curation [Equal], Writing—original draft [Equal], Writing—review & editing [Equal]), Goudarz Molaei (Writing—original draft [Equal], Writing—review & editing [Equal]), and Theodore Andreadis (Writing—original draft [Equal], Writing—review & editing [Equal]) We hope that ... The known unknowns of Powassan virus ecology
Doug E Brackney and Chantal B F Vogels
Journal of Medical Entomology, tjad095, https://doi.org/10.1093/jme/tjad095
Powassan virus (POWV; Family: Flaviviridae, Genus: Flavivirus ) is the sole North American member of the tick-borne encephalitis sero-complex. While associated with high rates of morbidity and mortality, POWV has historically been of little public health concern due to low incidence rates. However, ... Everglades virus: an underrecognized disease-causing subtype of Venezuelan equine encephalitis virus endemic to Florida, USA
Nathan D Burkett-Cadena and others
Journal of Medical Entomology, tjad070, https://doi.org/10.1093/jme/tjad070
Everglades virus (EVEV) is subtype II of the Venezuelan equine encephalitis virus (VEEV) complex (Togaviridae: Alphavirus), endemic to Florida, USA. EVEV belongs to a clade that includes both enzootic and epizootic/epidemic VEEV subtypes. Like other enzootic VEEV subtypes, muroid rodents are ... La Crosse virus neuroinvasive disease: the kids are not alright
Corey A Day and others
Journal of Medical Entomology, tjad090, https://doi.org/10.1093/jme/tjad090
La Crosse virus (LACV) is the most common cause of neuroinvasive mosquito-borne disease in children within the United States. Despite more than 50 years of recognized endemicity in the United States, the true burden of LACV disease is grossly underappreciated, and there remain severe knowledge gaps ... Emerging tickborne viruses vectored by Amblyomma americanum (Ixodida: Ixodidae): Heartland and Bourbon viruses
Alan P Dupuis and others
Journal of Medical Entomology, tjad060, https://doi.org/10.1093/jme/tjad060
Heartland (HRTV) and Bourbon (BRBV) viruses are newly identified tick-borne viruses, isolated from serious clinical cases in 2009 and 2014, respectively. Both viruses originated in the lower Midwest United States near the border of Missouri and Kansas, cause similar disease manifestations, and are ... The increasing threat of Rift Valley fever virus globalization: strategic guidance for protection and preparation
Seth Gibson and others
Journal of Medical Entomology, tjad113, https://doi.org/10.1093/jme/tjad113
Rift Valley fever virus (RVFV) (Bunyavirales: Phlebovirus ) is a prominent vector-borne zoonotic disease threat to global agriculture and public health. Risks of introduction into nonendemic regions are tied to changing climate regimes and other dynamic environmental factors that are becoming more ... Colorado tick fever virus: a review of historical literature and research emphasis for a modern era
Emma K Harris and others
Journal of Medical Entomology, tjad094, https://doi.org/10.1093/jme/tjad094 Colorado tick fever virus is an understudied tick-borne virus of medical importance that is primarily transmitted in the western United States and southwestern Canada. The virus is the type species of the genus Coltivirus (Spinareoviridae) and consists of 12 segments that remain largely ... Culicoides-borne Orbivirus epidemiology in a changing climate
Amy R Hudson and others
Journal of Medical Entomology, tjad098, https://doi.org/10.1093/jme/tjad098
Orbiviruses are of significant importance to the health of wildlife and domestic animals worldwide; the major orbiviruses transmitted by multiple biting midge ( Culicoides ) species include bluetongue virus, epizootic hemorrhagic disease virus, and African horse sickness virus. The viruses, insect ... Cache Valley virus: an emerging arbovirus of public and veterinary health importance
Holly R Hughes and others
Journal of Medical Entomology, tjad058, https://doi.org/10.1093/jme/tjad058
Cache Valley virus (CVV) is a mosquito-borne virus in the genus Orthobunyavirus (Bunyavirales: Peribunyaviridae) that has been identified as a teratogen in ruminants causing fetal death and severe malformations during epizootics in the U.S. CVV has recently emerged as a viral pathogen causing ... Jamestown Canyon virus comes into view: understanding the threat from an underrecognized arbovirus
John J Shepard and Philip M Armstrong
Journal of Medical Entomology, tjad069, https://doi.org/10.1093/jme/tjad069
This review examines the epidemiology, ecology, and evolution of Jamestown Canyon virus (JCV) and highlights new findings from the literature to better understand the virus, the vectors driving its transmission, and its emergence as an agent of arboviral disease. We also reanalyze data from the ... Snowshoe hare virus: discovery, distribution, vector and host associations, and medical significance
Edward D Walker and Thomas M Yuill
Journal of Medical Entomology, tjad128, https://doi.org/10.1093/jme/tjad128
Snowshoe hare virus (SSHV), within the California serogroup of the genus Orthobunyavirus , family Peribunyaviridae , was first isolated from a snowshoe hare ( Lepus americanus ) in Montana, United States, in 1959. The virus, closely related to LaCrosse virus (LACV) and Chatanga virus (CHATV), ...
⚠️ Rapport très important et approfondi de l’Anses qui conclut que le motif sanitaire ne justifie pas le classement des renards en « espèce susceptible d’occasionner des dégâts ».
Les experts démontent les croyances infondées sur la supposée dangerosité du renard.
— Hugo Clément (@hugoclement) August 1, 2023 ------- NDÉ Le rapport - Évaluation des impacts sur la santé publique de la dynamique des populations de renards - Anses - Agence nationale de sécurité sanitaire de l’alimentation, de l’environnement et du travail - version 1 (26-07-2023) https://anses.hal.science/anses-04171242
Extrait 4. CONCLUSIONS ET RECOMMANDATIONS DE L’AGENCE
L’Agence nationale de sécurité sanitaire de l’alimentation, de l’environnement et du travail endosse les conclusions et recommandations du GT « Renard » relatives à l’évaluation des impacts sur la santé publique de la dynamique des populations de renards.
L’Agence souligne l’importance de ne pas engager d’action spécifique pour faire varier les populations de renards, que ce soit à la hausse ou à la baisse, pour des motifs globaux de santé publique, humaine comme animale. Elle note à ce titre, non seulement l’inefficacité de telles mesures sur la transmission d’agents pathogènes, mais les effets possiblement contre-productifs d’une réduction des populations de renards sur cette transmission, à l’instar de la transmission d’Echinococcus multilocularis.
Ainsi, et sauf situations sanitaires très particulières nécessitant des mesures locales et ciblées, la réduction de populations de renards ne peut pas être envisagée comme option globale pour lutter contre un agent pathogène. Par conséquent, en l’état actuel des connaissances, l’Anses considère que le motif sanitaire ne justifie pas le classement ESOD des renards.
Par ailleurs, l’Agence note qu’une analyse socio-économique délimitée pourrait être menée, en particulier pour évaluer l’impact de l’échinococcose. Cependant, le rôle du renard ne saurait se réduire à son impact sur les zoonoses, et une analyse socio-économique devrait intégrer plus largement les différents rôles qu’il joue dans l’écosystème, notamment en évaluant précisément les pertes de gibier ou dans les élevages avicoles.
Enfin, dans une approche une seule santé (One Health), il importe de mieux connaître les modalités de transmission des agents pathogènes et les interactions entre renards, humains, et autres espèces domestiques et sauvages.
Pr Benoit Vallet
CITATION SUGGÉRÉE
- Anses. (2023). Avis relatif à l’évaluation des impacts sur la santé publique de la dynamique des populations de renards. (Saisine 2022-SA-0049). Maisons-Alfort : Anses, 15 p.
[Image] Carabasse Denis sur Twitter, 02.08.2023 : "@hugoclement @Nathanmg56 https://t.co/YpK2C4zUVK" https://twitter.com/DenisCarabasse/status/1686505607312846848
La mise en œuvre des politiques santé environnementale a souvent été abordée sous l’angle de la réduction des facteurs de risques environnementaux, notamment physiques (pollution atmosphérique, bruit, îlots de chaleur urbains, etc.). Or, la biodiversité, lorsqu’elle est associée à des écosystèmes fonctionnels et par les « services écologiques » qu’elle rend, pourrait participer d’une démarche de prévention et promotion de la santé. ORS - Observatoire régional santé, 08.02.2023 "À l’échelle globale, l’hypothèse selon laquelle le maintien de communautés biologiques présentant une diversité spécifique élevée permettrait, grâce à un « effet de dilution » d’éviter l’émergence de pathogènes majeurs susceptibles d’être à l’origine de zoonoses fait encore largement débat dans la sphère scientifique. Pour autant, à l’échelle plus locale, de nombreuses études attestent des bénéfices apportés par les écosystèmes sur la santé mentale et physique, notamment en matière de « nature en ville ».
Cependant, force est de constater que verdir n’est pas synonyme de renaturer et que les bénéfices des espaces à caractère naturel ne peuvent être associés uniquement au développement de son offre. Les bienfaits des espaces végétalisés sur la biodiversité et la santé dépendent également de la qualité écologique des milieux ou encore de la fréquentation de ces espaces.
L’impact de la végétation sur la réduction des nuisances environnementales telles que les vagues de chaleur, la pollution atmosphérique ou encore le bruit, n’est pas homogène et la renaturation ne peut se substituer à des actions de réduction à la source des polluants. Elle est en réalité complémentaire. L’efficacité des solutions de renaturation requiert une réflexion autour du choix des essences, du type de végétalisation, de leur emplacement géographique et de la surface du couvert végétalisé considéré ou encore de la disponibilité de l’eau. Outre les services de régulation apportés par les écosystèmes, il existe une littérature scientifique prolifique sur les bénéfices directs des espaces à caractère naturel en lien avec la stimulation de l’activité physique et la relation positive au « bien-être » au travers de bienfaits psychologiques, cognitifs et sociaux. Toutefois, tous les espaces verts ne constituent pas des lieux propices à la pratique d’activités qui dépend notamment de caractéristiques telles que leur accessibilité, leur surface, la sécurité des sentiers de marche, leur environnement sûr, l’ambiance paysagère, le soin apporté à leur entretien et les installations et équipements disponibles. Des réflexions sont à mener localement en croisant les expertises afin de préserver la biodiversité tout en garantissant l’accessibilité des populations les plus éloignées de la nature à ces espaces.
Dans ce rapport, nous avons souhaité nous arrêter sur deux enjeux autour desquels l’action publique relative à la santé humaine et la protection de la biodiversité ont tout intérêt à trouver des réponses communes : la production agricole et l’impact des pratiques de soin sur les écosystèmes." - Santé et biodiversité. Analyse des enjeux pour une approche intégrée en Île-de-France - 08 février 2023 → Consulter le rapport
Une équipe internationale de scientifiques vient d’utiliser les fourmis légionnaires comme « outil » d'échantillonnage des virus végétaux et animaux circulant dans une forêt profonde du Gabon. Cette approche innovante d’écologie virale ouvre la voie à une meilleure surveillance des zoonoses virales au niveau des écosystèmes forestiers tropicaux. Cirad 27 mars 2023 "L’originalité des travaux, publiés dans la revue Peer Community Journal, vient de l’idée d’utiliser les fourmis légionnaires comme relai d’échantillonnage des virus animaux et végétaux circulants dans un écosystème forestier tropical. Les colonies de fourmis légionnaires constituées de centaines de milliers d’individus effectuent des raids spectaculaires, chassant une très large gamme de proies vivantes, mais aussi dévorant des carcasses d'animaux ou se nourrissant directement de plantes. Cette étude de métagénomique virale a été produite par des équipes du Cirad, de l’IRD et d’INRAE en collaboration avec des partenaires sud-africains, américains, congolais et gabonais. Menés par Philippe Roumagnac et Eric Leroy, ces travaux montrent que les fourmis légionnaires peuvent accumuler une très grande diversité de séquences virales bactériennes, végétales, invertébrées et vertébrées. « Cette approche a permis de détecter chez les fourmis la présence de 157 genres viraux différents appartenant à 56 familles virales, ce qui est exceptionnel en termes de diversité virale », détaille Philippe Roumagnac, virologue au Cirad. Vers une surveillance précoce des zoonoses virales en milieu forestier tropical Ces travaux précurseurs représentent une première étape qui pourrait ouvrir la voie à des études à grande échelle sur le virome - ensemble des virus - de tous les écosystèmes forestiers tropicaux. Les fourmis légionnaires pourraient ainsi devenir des alliées de choix dans les travaux sur l’émergence des maladies et dans la surveillance précoce de virus zoonotiques pouvant passer de l’animal à l’humain et entrainer la survenue d’épidémies." [Image] Fourmis légionnaires. Crédit : Pierre Becquart, IRD
Researchers characterized the mammal-infecting viruses in 149 bats, representing six genera and 15 species, sampled from Yunnan province, China using an unbiased meta-transcriptomics approach. By Neha Mathur Nov 28 2022 Reviewed by Aimee Molineux Characterization of bat viromes reveals the co-infection, spillover, and emergence risk of several zoonotic viruses Image Credit: Rudmer Zwerver/Shutterstock ------- NDÉ Traduction Dans une étude récente publiée sur le serveur de préimpression bioRxiv*, des chercheurs ont caractérisé les virus infectant les mammifères chez 149 chauves-souris, représentant six genres et 15 espèces, échantillonnées dans la province du Yunnan, en Chine, en utilisant une approche méta-transcriptomique non biaisée. Traduit avec www.DeepL.com/Translator (version gratuite) ------- Dans la presse → Chine : un nouveau virus proche du covid découvert chez des chauves-souris - Geo.fr, 30.11.2022 https://www.geo.fr/environnement/chine-un-nouveau-virus-proche-du-covid-decouvert-chez-des-chauves-souris-212756 → Virus BtSY2 : les chercheurs alertent ! Un nouveau virus tueur de type corona découvert chez les chauves-souris [4 days ago]
https://news.dayfr.com/health/1360892.html → [...]
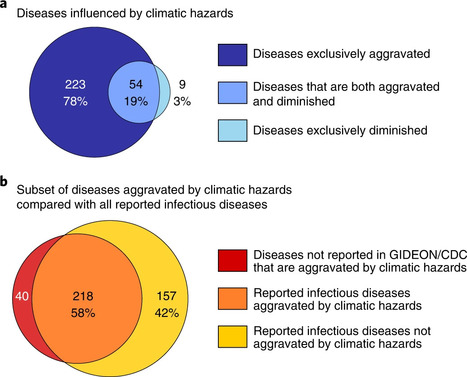
Le changement climatique perturbe la manière dont les agents infectieux se propagent. Une étude récente publiée dans Nature Climate Change vient de confirmer que plus de la moitié des maladies infectieuses ont déjà été aggravées par le réchauffement global de la planète. Dans ce contexte, les agents pathogènes risquent de s’adapter à la fièvre, l’un de nos meilleurs moyens de défense ! Publié le 05 Sep 2022 à 13H00 Modifié le 6 septembre 2022 Par Ives Etienne "... L’étude publiée par les chercheurs de l’université d’Hawaï aux États-Unis [...] donne des chiffres inquiétants : sur 375 types de maladies infectieuses étudiées, 218, soit 58 %, ont déjà été aggravées par le réchauffement climatique.
Le réchauffement climatique augmente la transmission des maladies infectieuses en élargissant la zone de répartition géographique de certains insectes et d’acariens. Ceux-ci peuvent transmettre des maladies parasitaires comme le paludisme, des maladies bactériennes comme la peste ou des maladies virales comme la dengue. Il s’agit de maladies dites vectorielles, car transmises par l’intermédiaire de vecteurs. Elles sont responsables actuellement de plus de 2,5 millions de décès par an.
L’augmentation de la température du globe a aussi un impact sur les zoonoses, des maladies infectieuses transmises par des animaux vertébrés à l’homme." (...) "Dans leurs travaux, les chercheurs préviennent aussi que l’augmentation de la température de la Terre provoque des extrêmes climatiques qui obligent l’organisme humain à s’adapter aux vagues de chaleur et au froid extrême. Cette lutte de l’organisme provoque un affaiblissement du système immunitaire et une plus grande sensibilité aux maladies. Ces organismes pathogènes risquent aussi de s’adapter à l’augmentation de température en mettant en péril la fièvre, l’un des mécanismes les plus fondamentaux du corps humain pour se défendre contre les infections." (À lire aussi : Réchauffement climatique : notre corps pourra-t-il supporter les augmentations de température ?) ---------- NDÉ Image tirée de l'étude : Diseases affected by climatic hazards https://www.nature.com/articles/s41558-022-01426-1/figures/4
Les tiques sont responsables de la transmission de nombreuses zoonoses, qui sont des maladies infectieuses transmises de
Les zoonoses sont des maladies infectieuses transmises de l’animal à l’homme ou vice et versa. Provenant le plus souvent de réservoirs animaux de la faune sauvage, les agents pathogènes zoonotiques peuvent être d’origine bactérienne, parasitaire ou virale. Elles sont responsables d’un grand nombre de maladies infectieuses nouvellement recensées ainsi que de maladies existantes. Après la pandémie de la Covid-19 qui a impacté le monde entier et causé la mort de plus de 13 millions de personnes selon l’OMS, les zoonoses constituent un problème majeur de santé publique. Académie nationale de médecine, 09.06.2022
"Depuis 1940, 60% des maladies infectieuses émergentes sont d’origine animale dont les 2/3 proviennent de la faune sauvage et les 4 dernières pandémies sont dues à des virus. Première pandémie de l’ère du numérique, la COVID-19 a occulté d’autres zoonoses majeures présentant des risques sanitaires importants.
L’Académie nationale de médecine a jugé nécessaire de créer une veille informationnelle sélective et structurée sur le risque zoonotique des zoonoses virales, qui n’existait pas jusqu’alors.
Cette veille, à l’attention des médecins, scientifiques, chercheurs, professionnels de la santé, de l’information et des pouvoirs publics, doit permettre d’accéder aux actualités sur ce sujet et d’être avertis immédiatement de toute alerte ou risque.
Grâce à la pluridisciplinarité des membres de l’Académie, cette veille s’inscrit dans le concept One Health impliquant les santés humaine, animale et environnementale." (...)
----------
AJOUT :
via Les zoonoses, quand les animaux contaminent l’Homme | Anses https://www.anses.fr/fr/content/les-zoonoses-quand-les-animaux-contaminent-l%E2%80%99homme
Comment se transmettent les zoonoses ? "Les modes de transmissions des zoonoses à l’Homme sont variés. Certains agents pathogènes se transmettent à l’occasion de contacts directs entre l’Homme et l’animal comme par exemple le virus de la rage ou de la grippe aviaire, certaines par l’intermédiaire de l’environnement, que ce soit par l’eau (bactéries et virus entériques) ou les sols (tétanos, maladie du charbon…). D’autres encore sont transmis par la consommation d’aliments d’origine animale contaminés, ou par les déjections (salmonelles, toxoplasme, ver parasite anisakis, etc.). Enfin, certaines zoonoses sont transmises par l’intermédiaire d’un arthropode vecteur tel que les moustiques ou les tiques, c’est le cas de la maladie de Lyme ou du virus West Nile." (...)
Les autorités sanitaires se veulent cependant rassurantes et précisent que le risque de transmission entre humains est faible. Le Monde avec AFP Publié le 28 avril 2022 à 17h29 "C’est la première fois qu’un cas de grippe aviaire est détecté chez l’humain. Un garçon de 4 ans, vivant dans la province du Henan, dans le centre du pays, a été testé positif à la souche H3N8, a annoncé le ministère de la santé chinois, mercredi 27 avril. L’enfant a été hospitalisé au début d’avril pour une fièvre et d’autres symptômes. Il avait été infecté directement par les oiseaux – sa famille élève des poulets et vit dans une zone peuplée de canards sauvages. Le ministère de la santé chinois appelle à ne pas s’approcher des oiseaux morts ou malades et à consulter en cas de fièvre ou de symptômes respiratoires. Toujours selon cette même source, cette contamination résulte d’une « transmission interespèces ponctuelle » et « le risque de transmission à grande échelle est faible ». Les tests effectués sur les personnes proches du malade n’ont d’ailleurs révélé « aucune anomalie ». Transmission très rare Des experts interrogés par le quotidien britannique The Guardian confirment cette analyse. « Il arrive souvent qu’un virus se propage à un humain puis s’arrête là. Un seul cas n’est pas une cause de grande inquiétude », a ainsi déclaré sir Peter Horby, professeur de maladies infectieuses émergentes et de santé mondiale à l’université d’Oxford. « Il n’y a aucune raison de penser que cela ira plus loin », a abondé le professeur Paul Digard du Roslin Institute de l’université d’Edimbourg. L’Organisation mondiale de la santé (OMS) va cependant mener une enquête sur ce cas « inhabituel », a annoncé le docteur John McCauley, directeur d’un centre de surveillance de la grippe collaborant avec l’OMS, au Guardian. Si les cas de transmission de grippe aviaire entre humains sont extrêmement rares, la souche H3N8 est connue pour se transmettre parmi les chevaux, les chiens et les phoques. Selon une étude américaine publiée en 2012 dans la revue Nature, la souche H3N8 aurait ainsi entraîné des pneumonies mortelles chez plus de 160 phoques le long des côtes américaines l’année précédente. Seules les souches H5N1 et H7N9, détectées respectivement en 1997 et 2013, ont été les principales à l’origine des cas humains de grippe aviaire, selon les Centres américains de contrôle et prévention des maladies (CDC)." Pour aller plus loin : "Les ténébrions sont des vecteurs connus de 60 maladies ou plus susceptibles de toucher les volailles, comme la maladie de Newcastle, la grippe aviaire, la maladie de Marek, la bursite infectieuse, Salmonella spp., 26 types pathogènes d'E. Coli, d'Eimeria spp. et d'Aspergillus, les parasites responsables de la coccidiose ainsi que les nématodes." "Alphitobius diaperinus, ou petit ténébrion mat, est l'un des organismes nuisibles les plus communs dans les poulaillers. Le petit ténébrion mat est parfois appelé ténébrion des poulaillers. Il se nourrit habituellement de grain, mais les poulaillers sont pour lui un environnement idéal où il peut prospérer en consommant les aliments déversés et le fumier sous les conduites d'alimentation. Lorsqu'il est présent dans les poulaillers, le petit ténébrion mat pose plusieurs difficultés économiques et liées à la biosécurité chez les producteurs de tout l'Ontario et de la plus grande partie de l'Amérique du Nord. Dans la présente fiche technique, on décrit le cycle biologique du ténébrion et on parle des différents modes de lutte contre cette espèce. (...) _______________________________ Les Ectoparasites aviaires "Les parasites externes des volailles ou « ectoparasites » peuvent être : - des insectes piqueurs et suceurs de sang : Les puces ;
- des insectes se nourrissant de débris tégumentaires : Les poux ;
- des acariens hématophages : Les poux rouges ;
- des acariens parasites des téguments : Les gales ;
- des acariens parasites de l'appareil respiratoire ;
- des champignons vivant aux dépens de téguments : Les teignes.
Le plus souvent, toute une population d'arthropodes commensaux vit autour des volailles dans
les bâtiments et la litière. Leur prolifération est source d'une gêne intense pour les oiseaux :
- allergies intestinales avec entérite et diarrhée dues aux acariens ;
- gêne cutanée avec grattage voire picage lors d'invasions massives des litières par des acariens ;
- gêne zootechnique (baisse des performances) par les proliférations intenses de tous les acariens ;
- transport de virus, bactéries et autres parasites sources de contamination pour les oiseaux.
D’autres insectes sont à prendre en considération : c’est le cas du ténébrion et des mouches, qui sont un véritable fléau et vecteurs de la maladie de Marek, de la maladie de Gumboro et d’autres viroses aviaires."
Dr LEZZAR Nawel Maitre de Conférences - Spécialiste en Aviculture et Pathologie Aviaire - Année universitaire 2017-2018 _______________________________ "... La zoonose virale d’origine aviaire la plus connue fut pendant de nombreuses années la maladie de Newcastle jusqu'à l'émergence du virus influenza A hautement pathogène de sous-type H5N1 (IAHP H5N1) en Asie. D'autres virus sont zoonotiques mais le plus souvent ils sont hébergés par les oiseaux sauvages et transmis à l'Homme par des vecteurs. Orthomyxovirus: virus Influenza A hautement pathogène ou IAHP (peste aviaire) Avant 1997, où des cas humains liés à l’influenza aviaire H5N1 ont été signalés à Hong Kong (18 cas dont 6 décès), seule la grippe porcine était considérée comme une zoonose. Depuis, nous savons qu'il existe un risque de zoonose avec les virus IAHP de sous-types H5N1 (appelée par les médias «grippe aviaire»), H9N2 et H7N7."
La question de l’origine du Covid-19 occupe une place centrale dans la médiatisation inédite de la pandémie. Et questionne la manière dont les politiques de santé publique doivent s’orienter. Philippe Grandcolas 2 janvier 2022, 18:25 CET • Mis à jour le 4 janvier 2022 "Le Covid-19 est probablement la pandémie et la maladie infectieuse la plus médiatisée de tous les temps. D’autres zoonoses – ces maladies dont l’agent infectieux est issu d’un animal – ont eu aussi un grand retentissement sociétal, comme le sida (virus HIV) qui tue encore plus d’un demi-million de personnes par an dans le monde. Et d’autres maladies tout aussi terribles, comme le paludisme ou Ebola, frappent tout particulièrement les régions tropicales et on peut regretter qu’elles n’inquiètent guère les habitants et les dirigeants des puissants pays du Nord. Émergence du Covid-19, à chacun son hypothèse ! La question de l’origine du Covid-19 a une part importante dans la médiatisation inédite de la pandémie. Les hypothèses se sont multipliées, évoquant aussi bien le passage naturel à l’humain depuis une chauve-souris – avec ou sans hôte intermédiaire (pangolin, civette, vison, chien viverrin, etc.) – que l’échappement d’un laboratoire de virologie dans la ville chinoise de Wuhan. Chaque « corporation » y a été de son hypothèse : les scientifiques écologues, dont je suis, ont replacé l’émergence du Covid-19 dans le contexte de l’augmentation inquiétante des émergences de nouvelles maladies zoonotiques, causées par les atteintes à l’environnement. Des journalistes ont alerté sur le rôle possible des élevages animaux (notamment de visons) comme réacteurs de sélection d’agents infectieux. Quant aux biologistes moléculaires de laboratoire qui utilisent la transgenèse (insertion de gènes au sein de virus) comme outil de travail quotidien pour comprendre la fonction de gènes ou de protéines spécifiques des virus, ils se sont inquiétés du manque de transparence des travaux menés dans les laboratoires de Wuhan en Chine, ville présumée à tort ou à raison lieu d’émergence de la pandémie. Chacun voit donc midi à sa porte, en émettant le souhait (très idéalisé) d’un meilleur comportement dans son domaine sociétal d’intérêt. Bien que de moindre intérêt, on peut également mentionner le développement de nombreuses publications, passablement complotistes, qui traquent les informations disponibles dans les courriers et documents des différents acteurs du domaine (groupes de recherche, OMS, chercheurs, etc.) ; et pensent y trouver les preuves de méfaits ou d’imprudences expliquant l’émergence de la maladie. Enfin, pour compléter cette liste déjà trop longue, on doit aussi signaler des épisodes de politique internationale incriminant tel ou tel personnage ou institution, à tort ou à raison, mais pour des raisons d’adversité politique. Le concept central d’« une seule santé » Que penser de toutes ces hypothèses ? En fait, chacune d’entre elles, sauf sans doute celle de l’origine naturelle, fait passablement l’impasse sur les démarches scientifiques intégratives qui sont le futur indispensable des recherches sur les maladies infectieuses. Depuis des années maintenant, biologistes et médecins ont forgé en recherche scientifique le concept d’« une seule santé » (One Health) : la santé humaine dépend de celle de l’environnement et de celle des autres animaux. Ce concept prend ainsi en compte toutes les hypothèses formulées pour permettre de juger à terme de leur vraisemblance à la lumière des éléments recueillis : agents infectieux inconnus ou émergents (virus, bactéries, protozoaires, etc.) dans leurs animaux réservoirs, rôle des élevages et trafics (qui concentrent et affaiblissent ces animaux réservoirs) ; enfin, rôle des laboratoires de biologie médicale qui devraient étudier cette problématique sans générer de risques supplémentaires. À ce dernier égard, il est particulièrement ironique de constater que les tenants des fuites de laboratoire de Wuhan mentionnent eux-mêmes la nécessité de juger du rôle des protéines spike des nouveaux variants (Omicron notamment) en les étudiant leur biologie grâce à la transgenèse dans des lentivirus. Les expertises collégiales nationales (FRB) et internationales (IPBES) mentionnent toutes cette exigence absolue d’intégration « une seule santé » pour comprendre et juguler l’émergence de maladies dans le futur ! Les humains ne vivent pas en vase clos et leur santé dépend évidemment de celle de leur environnement : il faut sans cesse le rappeler tant nos attitudes demeurent anthropocentriques et centrées sur les remèdes a posteriori chez les humains plutôt que sur les études intégratives a priori des crises sur les écosystèmes. À la recherche de nouvelles connaissances cruciales Pour prévenir l’émergence de nouvelles maladies, nous sommes donc directement dépendants des connaissances que nous avons sur la biodiversité : celle des agents infectieux et celle des animaux réservoirs. Chaque étude récente de l’évolution des coronavirus montre que nous ne connaissons que des parents proches, mais pas immédiats, du SARS-CoV-2, tous localisés dans l’Asie du Sud-Est où l’origine de la maladie peut donc être vraisemblablement située. À cet égard, l’émergence présumée à Wuhan (province d’Hubei) doit être réinterprétée en regard des détections bien plus précoces de la maladie déjà transmise en plusieurs points du globe, et notamment en Europe (dans cette étude française notamment). Cela signifie que les parents et précurseurs du SARS-CoV-2 ne sont pas encore connus et se trouvent quelque part dans des animaux ou humains de cette région. Depuis le début de la pandémie, de nouveaux résultats importants ont été acquis, avec la découverte de nouveaux coronavirus en Thaïlande, au Cambodge et au Laos. Ces études sont cruciales, car elles permettent de dessiner à grands traits l’évolution de ces virus et de leurs caractéristiques biologiques. D’autres coronavirus déjà connus de chauve-souris rhinolophes, par exemple en Russie, ont été par ailleurs testés pour leur capacité malheureusement positive à se fixer sur les protéines des cellules humaines et donc à constituer un risque potentiel. Pour comprendre comment lutter efficacement contre le virus, il est en effet important de savoir sous quels régimes de sélection naturelle ces traits originels sont apparus. Pour empêcher de futures émergences, il est également primordial de connaître les animaux réservoirs impliqués et les éventuels hôtes intermédiaires. La quête de l’origine Comme tout un chacun le perçoit désormais, les virus évoluent rapidement et ce que l’on appelle « variants » sont le résultat de mutations apparaissant et se transmettant dans des populations colossales de virions. Pour mémoire, un malade infecté héberge de 1 à 100 milliards de virions (nombre total de particules virales). La population mondiale de SARS-CoV-2 compte donc des milliards de milliards de virions, issus d’autant d’épisodes de réplications dans nos corps avec à chaque fois la possibilité d’apparitions et de transmissions de mutations ! Mais l’origine de certains virus peut aussi être recherchée dans des évènements de recombinaisons entre virions occupant les mêmes cellules de leur hôte, et générant des mosaïques à partir de virions différents. Si l’on ne connaît pas raisonnablement les virus dans la nature, il est illusoire de penser comprendre un jour leur origine. Il a ainsi fallu quatorze ans pour identifier une localité en Asie d’où était issu le virus du premier SARS qui, bien que moins pandémique, avait tout de même touché au moins 8000 personnes et causé plus de 700 décès dans huit pays différents. Récemment encore, on s’est aperçu que le virus Ebola pouvait resurgir dans des populations humaines à la suite d’une « dormance » chez un individu apparemment « porteur sain ». Et certains biologistes imaginent actuellement que des variants très modifiés (comme Omicron) pourraient apparaître soudainement dans des populations humaines à la suite d’une longue évolution dans le corps de malades immunodéprimés, une hypothèse néanmoins très spéculative… La biologie de terrain des virus et de leurs réservoirs est donc fondamentale à toute politique de santé publique. Aujourd’hui, de nombreuses équipes recherchent activement les précurseurs du SARS-CoV-2, mais encore sans succès immédiat. Le Covid-19, une zoonose parmi d’autres Il est désormais essentiel que la focalisation médiatique sur le Covid-19 ne devienne pas l’arbre qui cache la forêt. Depuis 1940, le nombre d’émergences de maladies infectieuses ou de pic épidémiques a augmenté considérablement, et chacun a entendu le nom de plusieurs d’entre elles, apparues ou devenues épidémiques récemment : sida, Ebola, Nipah, MERS, SARS, maladie de Lyme, Zika, virus du Nil occidental, etc. La fragmentation et la conversion effroyable des milieux, avec des millions d’hectares de forêts tropicales disparaissant chaque année, nous met en contact croissant avec la faune sauvage et donc les animaux réservoirs qui sortent du bois. La croissance exponentielle des centres urbains, les braconnages et trafics générés, les élevages industriels aux conditions sanitaires désastreuses et, enfin, les transports internationaux en croissance folle, représentent autant de facteurs de transferts d’agents infectieux vers les humains et d’émergence de maladies. Voir la question des zoonoses émergentes uniquement comme un problème de gestion de laboratoire de recherche à Wuhan serait, on le comprend, très dangereusement réducteur. Une telle focalisation nous empêcherait de prêter attention à tous les problèmes existants ou en devenir de santé environnementale. Près de nous, en Europe, qui se soucie par exemple de la maladie de Lyme, de la toxoplasmose ou de la leptospirose, alors que leur impact et leur gestion sont problématiques ? Ces agents infectieux ne se sont pas échappés de laboratoires mal gérés ! En 2022 comme à plus long terme, prendre en compte l’état de l’environnement doit rester une problématique majeure des politiques de santé publique." À lire aussi : → Origine de la Covid-19 : l’hypothèse de l’accident de laboratoire doit-elle être étudiée d’un point de vue scientifique ? → Il y a 10 ans, un virus proche du SARS-CoV-2 circulait déjà au Cambodge → Les clés pour empêcher les futures pandémies [Image] Vue au microscope de cellules infectées par le SARS-CoV-2. BEN STANSALL / AFP
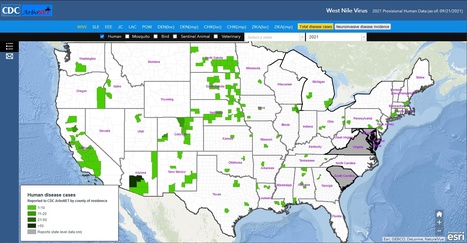
L’infection par le virus West Nile, également appelé virus du Nil occidental, est une zoonose connue en France depuis les années 1960 et dont la diffusion à l’échelle de la planète s’est modifiée récemment. Fièvre du Nil occidental ou infection par le virus West Nile Santé ,publique France, mise à jour du 24.05.19 Epidémiologie Le virus West Nile, qui avait auparavant été responsable d’épidémies en Afrique, Europe de l’est, au Moyen Orient et en Asie, a été détecté pour la première fois sur le continent américain, aux États-Unis, en 1999. Depuis, il diffuse à tout le continent nord américain où la maladie se présente comme une maladie émergente. En date du 21 septembre 2021, un total de 479 cas d'infection humaine par le virus du Nil occidental a été signalé aux CDC. Parmi ceux-ci, 315 (66 %) ont été classés comme des maladies neuro-invasives (telles que la méningite ou l'encéphalite) et 164 (34 %) ont été classés comme des maladies non neuro-invasives. [Image] National & state maps (including county-level data) from 2003 – present. _____________________________ actualité repérée via News 24, 22.09.2021
https://news-24.fr/la-propagation-mortelle-du-virus-du-nil-occidental-qui-a-tue-19-personnes-a-travers-lamerique-revelee-sur-une-carte-effrayante/
"Tout le monde a déjà entendu parler de la maladie de Lyme. Mais saviez-vous qu’il existe de nombreuses espèces de tiques en France, et qu’elles propagent d’autres maladies, dont certaines émergentes ?" Nathalie Boulanger, 28.06.2021 "Sur les 900 espèces de tiques que l’on trouve dans le monde, une quarantaine vit en France. La plus connue d’entre elles est probablement la tique Ixodes ricinus, largement médiatisée en raison de son rôle dans la propagation de la maladie de Lyme. En revanche, on sait peut-être moins que cette espèce transmet également d’autres maladies, et que d’autres tiques peuvent également piquer l’être humain, quoique plus rarement. Petit inventaire des tiques « françaises » et des problèmes qu’elles peuvent causer. Les tiques les plus importantes pour la santé humaine en France Les tiques se répartissent en deux familles principales, les tiques dures (ou Ixodidae) et les tiques molles (ou Argasidae). Mais qu’elles soient dures ou molles, une fois sorties de leur œuf, toutes se développent de la même façon, en passant par trois étapes, ou stases : la larve, la nymphe et l’adulte (mâle ou femelle). Entre chaque stase, un repas sanguin est nécessaire pour induire la mue qui permettra de passer à l’étape suivante. C’est à ce moment que les tiques peuvent, si elles se nourrissent sur un animal infecté, acquérir un micro-organisme potentiellement pathogène (parasite, virus ou bactérie). Elles deviennent alors susceptibles de le transmettre à un nouvel hôte, animal ou humain, lors du repas de sang suivant. Les tiques molles piquent rarement l’être humain. La tique du pigeon, Argas reflexus, est celle qui est le plus souvent incriminée. Cette tique prend un repas sanguin court, généralement la nuit. Jusqu’à présent, son implication dans la transmission de maladies à l’homme n’a pas été démontrée. En revanche, sa salive peut induire des chocs anaphylactiques, autrement dit des réactions allergiques violentes lesquels peuvent entraîner des pertes de connaissances, voire nécessiter une prise en charge en réanimation. En ce qui concerne les tiques dures, les genres les plus importants sont : Ixodes, Dermacentor et Rhipicephalus (Figure 1). Leurs repas, plutôt pris en journée, sont longs : ils durent de 3 à 10 jours. Ces tiques sont vectrices d’un grand nombre d’agents potentiellement infectieux : des bactéries (Borrelia, Anaplasma, Rickettsia…), des virus tels que le virus de l’encéphalite à tique voire des parasites comme Babesia. Les maladies à tiques sont en majorité des zoonoses : les agents infectieux qui les causent sont transmis à l’être humain à partir des animaux. Cette transmission est « accidentelle », dans le sens où l’humain n’est pas habituellement un hôte de ces micro-organismes ; se retrouver dans notre corps signifie pour eux arriver dans une impasse, puisque nous ne faisons pas partie de leur cycle de reproduction." (...) [Image] Face dorsale des principaux genres Ixodidae (tiques dures) et Argasidae (tiques molles) d’importance médicale et vétérinaire en France. Photos de la collection personnelle JM Berenger, URMITE, Marseille, Author provided
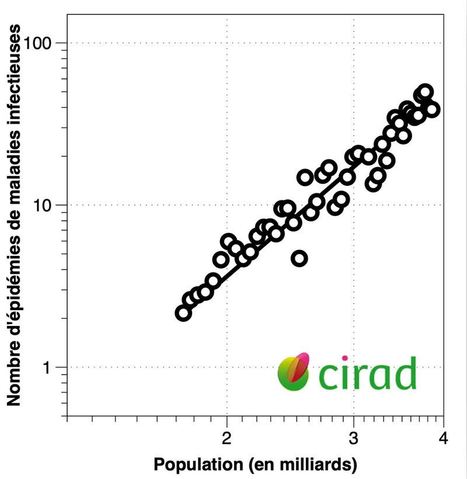
L’hypothèse d'un lien direct entre déforestation et émergence de zoonoses s’est imposée médiatiquement, puis a été reprise par les politiques, alors qu’elle n’a jamais été prouvée scientifiquement. Par Jacques Tassin et Jean-Marc Roda, 19.03.2021 "... la date d’émergence de tout nouveau virus reste elle-même incertaine. On ne sait toujours pas quand le virus VIH est apparu chez l’être humain, si ce n’est que l’horloge moléculaire situe son origine dans les années 1940 avec une incertitude d’une quinzaine d’années. On ne sait pas non plus à quand remonte l’apparition du SARS-CoV-2, mais certains indices permettent d’imaginer que ce virus pourrait déjà avoir été présent chez l’être humain en 2012. Dans ces conditions, il est d’autant plus difficile d’établir des liens de causalité. En écologie, il faut se méfier des « coupables idéaux » Autre difficulté : en écologie, on sait qu’une tendance valable à une échelle peut s’inverser à une autre : par exemple, un milieu est d’autant plus « invasible » qu’il est pauvre en espèces à l’échelle d’une placette de quelques mètres carrés, mais qu’il est riche à l’échelle d’un paysage ou d’une région. Cela a tout particulièrement été observé pour les plantes aquatiques, mais s’étend à l’ensemble du monde végétal. Dans ces conditions, à quelle échelle de temps et quelle échelle spatiale (du local au régional) faut-il se positionner quand on veut estimer le rôle de la déforestation ? L’écologie, science de la complexité par excellence, s’accommode mal de simplismes. Tous les éléments que nous avons cités révèlent que le lien supposé entre la déforestation et l’émergence de zoonoses est non seulement hypothétique, mais indémontrable. Partant de ce constat, il serait d’autant plus regrettable de s’enfermer dans cette unique voie explicative sans issue alors que nous savons, sur des bases statistiques irréfutables, que l’apparition des zoonoses est directement liée à la précarité et à l’insalubrité, à la concentration des habitations, à la mobilité humaine, à la taille de la population. Mettre en lien la déforestation et les zoonoses n’est donc pas anodin, ni sans conséquence. Il ne s’agirait pas d’oublier, en premier lieu, que toutes résultent des mêmes causes : les conditions d’insalubrité et la précarité des populations rurales des zones tropicales. C’est la recherche de terres à cultiver et de protéines de brousse, par une population mondiale en situation de grande précarité et d’insalubrité, qui constitue le moteur originel de la disparition des forêts tropicales et de l’émergence des zoonoses. En définitive, toute cette problématique est sous-tendue par notre terrible indifférence initiale à la situation rurale mondiale…" [Image] Le nombre d’épidémies infectieuses et la taille de la population des pays de la région Asie-Pacifique se révèlent très fortement liés) CIRAD, Jean‑Marc Roda, à partir des données de FAOSTAT et GIDEON (échelles logarithmiques) _________________________________________ Lien ci-dessus : → Les silences de la Chine, un virus repéré dès 2013, la fausse piste du pangolin... Enquête sur les origines du SARS-CoV-2. Par Stéphane Foucart, 23.12.2020 https://www.lemonde.fr/sciences/article/2020/12/22/a-l-origine-de-la-pandemie-de-covid-19-un-virus-sars-cov-2-aux-sources-toujours-enigmatiques_6064168_1650684.html
|
Quatre types d'infections virales transmises de l'animal à l'humain (anthropozoonose) ont augmenté à un rythme exponentiel, les épidémies devenant généralement plus importantes et plus fréquentes au cours des 60 dernières années. Guru Med | 8 Nov 2023 "Des scientifiques de la société américaine de biotechnologie Ginkgo Bioworks, fondée par cinq scientifiques du MIT, affirment que si les tendances actuelles se maintiennent, les zoonoses devraient collectivement tuer 12 fois plus de personnes en 2050 qu’elles ne l’ont fait en 2020. Les résultats présentés dans une nouvelle étude (lien plus bas) proviennent d’une analyse de plus de 3150 foyers et épidémies entre 1963 et 2019."
#RETRO | Et si les fourmis légionnaires se révélaient être de précieuses alliées pour surveiller l'émergence de #zoonoses ?
Une équipe internationale de scientifiques les a utilisées comme « outil » d'échantillonnage de virus végétaux et animaux Cirad (@Cirad) July 27, 2023 ------- NDÉ Illustration [Image] Fourmis légionnaires, et chasseuses de virus ! Crédits : AFP - CYRIL RUOSO - BIOSPHOTO - BIOSPHOTO VIA AFP
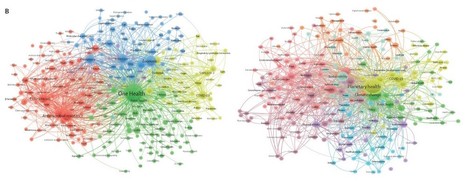
The COVID-19 pandemic and the anthropogenic impact on Earth's life-support systems and planetary boundaries have reinvigorated the One Health and planetary health concepts, propelling them to the forefront of the global health and sustainable development agendas. Although both concepts build on equivalent systemic principles, there is an ongoing debate and emerging confusion around their differences and application areas.1–3 One Health and planetary health research: leveraging differences to grow together Castañeda RR, Viller J, Guzmán CAF, Eslanloo T, de Paula N, Machalaba C, Zinsstag J, Flahault A, Bolon I, The Lancet, Vol 7, Issue 2, Feb 2023
[Image] All topics related to infectious diseases were the most represented in One Health publications (eg, COVID-19, antimicrobial resistance, and zoonoses; figure B) ------- NDÉ Traduction "..... La santé animale, en particulier les zoonoses (par exemple, la résistance aux antimicrobiens et les maladies infectieuses émergentes), reste le domaine de recherche One Health le plus important, tandis que la recherche en santé planétaire ne traite pas de la santé animale. La santé planétaire se concentre davantage sur l’environnement, en particulier les changements climatiques et la santé humaine, ainsi que sur les déterminants sociaux de la santé humaine. Pourtant, le changement climatique n’est pas unique à la recherche en santé planétaire, et nous observons des chevauchements croissants avec l’élargissement de One Health.
Ces chevauchements peuvent générer de la confusion, et il serait utile de clarifier davantage l’orientation relative de One Health et de la recherche en santé planétaire, principalement parce qu’ils impliquent souvent des disciplines et des communautés différentes.
Pourtant, cette diversité ne devrait pas être une raison de diverger ou de rivaliser, mais de collaborer.
Dans l’ensemble, One Health et la santé planétaire sont des domaines de recherche scientifique hautement complémentaires avec un solide levier pour la traduction en politiques et en pratiques. Il est possible de bâtir une communauté de recherche plus forte et des données probantes transdisciplinaires pour aborder collectivement les problèmes urgents de santé publique et mondiale d’une manière véritablement intégrée.
Par-dessus tout, la vie sur Terre est en danger, et notre diversité ne fera que nous rendre plus forts. »
via ONE HEALTH COMMISSION | LinkedIn
After 2 years of the COVID-19 pandemic, translating One Health into action is urgent The Lancet
Viewpoint
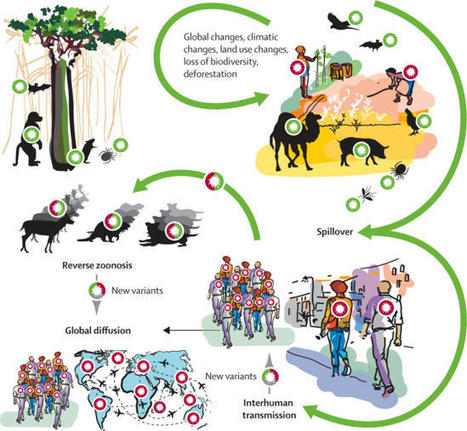
Available online 24 October 2022 AUTHOR(S) Lefrançois, Thierry; Malvy, Denis; Atlani-Duault, Laetitia; Benamouzig, Daniel; Druais, Pierre-Louis; Yazdanpanah, Yazdan; Delfraissy, Jean-François; Lina, Bruno [Image] Transmission of zoonotic diseases ------- NDÉ Traduction Le monde fait face aux conséquences sanitaires, sociétales et économiques de plus de deux ans de pandémie de COVID-19. Des maladies émergentes causées par de nouveaux agents pathogènes, ou maladies infectieuses réémergentes, apparaissent régulièrement et leur fréquence augmente. Plusieurs travaux de recherche ont montré que le coût de la prévention d'une maladie infectieuse est bien inférieur à celui de sa gestion, en particulier au niveau mondial. Un changement du cadre des soins de santé est nécessaire pour améliorer la prévention des pandémies, ce qui exigera une compréhension globale de l'émergence des maladies et une approche intégrée "One Health". Les facteurs environnementaux, sociaux, économiques, éthiques et politiques qui caractérisent un écosystème social et influencent l'émergence des zoonoses doivent être pris en compte pour contrôler ces émergences. Traduit avec www.DeepL.com/Translator (version gratuite)
" Le GBIF (Global Biodiversity Information Facility ou Système mondial d'information sur la biodiversité) est un réseau international dont le but est de mettre à disposition le maximum de données primaires sur la biodiversité via le portail www.gbif.org, de façon libre et gratuite. " 2 septembre 2022 Ces données primaires, aussi appelées données d’occurrences d’espèces, permettent de détailler où, quand, comment et par qui des représentants de toutes sortes d’espèces animales, végétales et d’autres groupes taxonomiques ont été observés ou collectés. Ces informations peuvent également prendre la forme de listes d’espèces ou d’échantillonnages naturalistes. L’INPN, plateforme nationale du Système d’information de l’inventaire du patrimoine naturel (SINP), contribue au GBIF depuis plusieurs années, en partageant au niveau international les données d’occurrences d’espèces rassemblées par les producteurs de données français de métropole et d'outre-mer. Ces données d’observation d’espèces sont transmises par les partenaires (associations naturalistes, bureaux d’études environnementales, services de l'État...), que ce soit au niveau régional grâce au travail des plateformes régionales du SINP et de leurs réseaux, mais également grâce aux réseaux de production nationaux. Cette contribution a encore augmenté en 2022 avec la diffusion vers le GBIF de plus de 19 millions de nouvelles données, portant à 101 millions le total des données partagées par PatriNat dans ce système d’information mondial sur la biodiversité ; cela fait de la France le 3e pays contributeur en termes de nombre de données partagées, issues de plusieurs centaines de producteurs. Cette contribution 2022 vers le GBIF a été marquée par l’ajout des données provenant des études d’impacts environnementaux et des projets d’aménagements concernés par le dispositif DEPOBIO, qui gère le dépôt légal des données brutes de biodiversité issues du secteur privé. Cela représente plusieurs milliers de nouveaux jeux de données sur tous les territoires français, qui viennent enrichir la connaissance des espèces au niveau national et international. Toutes ces données librement accessibles contribuent à la production de nouvelles études scientifiques ainsi qu’à l’appui aux politiques publiques : suivi des espèces envahissantes et des zoonoses, identification des zones à protéger en priorité, étude de la répartition et de la migration des espèces, etc. L’utilisation des données mises en ligne sur GBIF.org est compilée chaque année dans la revue scientifique du GBIF. Le GBIF France, en association avec PatriNat dans laquelle il est intégré, remercie tous les producteurs et éditeurs de données français ayant contribué au GBIF et reste disponible à l'adresse gbif@gbif.fr pour accompagner la mise en ligne ou l'utilisation des données accessibles dans le réseau GBIF ! En savoir plus - Voir la page data publisher de PatriNat sur gbif.org
- Voir la Revue scientifique du GBIF
- Voir le site du dispositif DEPOBIO
Voir la vidéo « Le SINP et la sphère internationale » décrivant les flux de données entre SINP et GBIF
Voir le Guide d’accompagnement pour la transmission des données d’observation sur les espèces dans le cadre de programmes nationaux Crédits photos Rosalie des Alpes Rosalia alpina : Julien Touroult
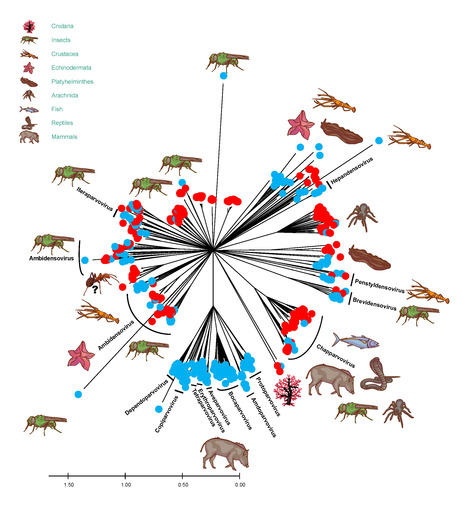
A new modeling tool from UC Davis helps prioritize novel and known viruses for zoonotic risk. It shows coronaviruses are riskiest for spillover to humans. A new modeling tool from UC Davis helps prioritize novel and known viruses for zoonotic risk. It shows coronaviruses are riskiest for transmission to humans. Novel Coronaviruses Are Riskiest for Spillove by Kat Kerlin August 25, 2022 ---------- NDÉ Traduction : Au cours de la dernière décennie, les scientifiques ont décrit des centaines de nouveaux virus susceptibles de passer de la faune sauvage à l'homme. Mais comment peuvent-ils savoir quels sont les virus les plus susceptibles de se propager et, par conséquent, ceux qu'il convient de surveiller en priorité chez l'homme ? Des scientifiques de l'université de Californie, à Davis, ont créé des modèles basés sur des réseaux pour classer les virus nouveaux et connus en fonction de leur risque de transmission zoonotique, c'est-à-dire lorsque des maladies infectieuses passent entre les animaux et les humains. Leur étude, publiée dans la revue Communications Biology, apporte des preuves supplémentaires que les coronavirus sont les plus susceptibles de se propager et qu'ils doivent continuer à faire l'objet d'une surveillance et d'une recherche accrues. Les modèles d'apprentissage automatique ont été conçus par l'EpiCenter for Disease Dynamics de l'UC Davis One Health Institute de l'école de médecine vétérinaire. Changement environnemental et connexions virales Le modèle utilise un réseau virus-hôte basé sur des données pour quantifier la probabilité que les humains soient les hôtes de plus de 500 virus nouvellement découverts entre 2009 et 2019. Ces données sont issues de recherches sur la surveillance de la faune sauvage menées en Afrique, en Asie et en Amérique latine par un consortium de chercheurs." [Image] Illustration du réseau hôte-virus montrant des points de petite et grande taille reliés par des lignes de différentes couleurs.
Cette illustration représente un modèle de réseau hôte-pathogène créé par des chercheurs de l'UC Davis. Elle montre les liens potentiels entre 531 nouveaux virus et des virus connus, les différentes couleurs représentant les différentes familles de virus. (UC Davis) L'étude : Extrait : Hiérarchisation des nouveaux virus pour une caractérisation plus poussée Pour les 531 nouveaux virus, nous avons élaboré des mesures de hiérarchisation qui renseignent sur les tendances écologiques et évolutives de la propagation en fonction du nombre de liens humains avec des virus connus prédits par le modèle multiclasse. Les nouveaux virus des familles Herpesviridae, Rhabdoviridae, Coronaviridae, Adenoviridae, Astroviridae, et Paramyxoviridae ont non seulement montré une probabilité médiane élevée de partager des liens humains avec des virus connus mais ont également été prédits comme ayant un grand nombre de liens humains dans le réseau prédit (Gpredicted). Les nouveaux virus des familles Picobirnaviridae et Rhabdoviridae détectés ici ont été considérés comme des hyperparasites infectant des bactéries et des insectes et ont été identifiés dans des échantillons de mammifères hôtes. Par conséquent, les associations prédites pour ces familles de virus ne doivent pas être déduites comme une infection mais seulement comme une détection dans des échantillons d'hôtes (par exemple, des virus d'insectes potentiellement détectés dans des échantillons d'écouvillons oraux de chauves-souris).
Emerging infectious diseases (EIDs), especially those with zoonotic potential, are a growing threat to global health, economy, and safety. Climate change and zoonoses: A review of the current status, knowledge gaps, and future trends - ScienceDirect Acta Tropica Volume 226, February 2022 Ruwini Rupasinghea, Bruno B.Chomelb, BeatrizMartínez-Lópeza - a
- Center for Animal Disease Modeling and Surveillance (CADMS), Department of Medicine and Epidemiology, University of California, Davis, CA, USA
- b
- Department of Population Health and Reproduction, School of Veterinary Medicine, University of California, Davis, CA, USA
---------- NDÉ Traduction : - Le changement climatique favorise les épidémies zoonotiques en modifiant les interactions hôte-pathogène.
- Nous avons examiné les prévisions de divers risques zoonotiques fondées sur le changement climatique futur.
- Le changement climatique peut provoquer une expansion vers les pôles et des changements saisonniers de certaines maladies.
- Recherches limitées sur les impacts des incendies de forêt sur les zoonoses.
- Nécessité d'ajouter des facteurs de risque socio-économiques dans les modèles pour de meilleures prédictions. Résumé Les maladies infectieuses émergentes (MIE), en particulier celles à potentiel zoonotique, constituent une menace croissante pour la santé, l'économie et la sécurité mondiales. L'influence du réchauffement climatique et des variations géoclimatiques sur l'épidémiologie des maladies zoonotiques est évidente par les modifications de la dynamique des hôtes, des vecteurs et des pathogènes et de leurs interactions. L'objectif de cet article est de passer en revue la littérature actuelle sur les impacts observés du changement climatique sur les zoonoses et de discuter des tendances futures. Nous avons évalué plusieurs modèles climatiques afin d'évaluer les projections de diverses zoonoses induites par les variations climatiques prévues. De nombreuses projections climatiques ont révélé une expansion géographique potentielle et la gravité des zoonoses à transmission vectorielle, hydrique, alimentaire, par les rongeurs et par l'air. Cependant, il existe encore des lacunes dans les connaissances et des recherches supplémentaires doivent être menées pour comprendre pleinement l'ampleur et les conséquences de certains de ces changements. Il est certain qu'en comprenant l'impact du changement climatique sur l'émergence et la distribution des zoonoses, nous pourrons mieux planifier les stratégies d'atténuation et d'adaptation au climat. Traduit avec www.DeepL.com/Translator (version gratuite) [Image] Impacts of global warming and geoclimatic variations on zoonoses.
Quel est le point commun entre l’écureuil à ventre rouge, la carpe argentée, le cygne noir, la grenouille taureau et la jacinthe d’eau ? Aucun n’évolue d’ordinaire en France. Il s’agit d’animaux et de plantes introduits volontairement ou involontairement sur un territoire hors de leur aire de répartition naturelle, et dont la propagation, corrélée à l’intensification des échanges commerciaux, à la dynamique et aux tendances démographiques, représente une menace potentielle pour les écosystèmes, les espèces endémiques (particulièrement des milieux insulaires), l’économie (rendements agricoles, foresterie) et la santé humaine (vecteurs de zoonoses et de pathogènes)." par Aurore Coulaud
publié le 17 mai 2022 (abonnés)
"D’après la Plateforme intergouvernementale scientifique et politique sur la biodiversité et les services écosystémiques, près du cinquième de la surface terrestre est menacé par des invasions végétales et animales. Des griefs qui valent à ces «nouveaux nuisibles» d’être classés comme «espèces exotiques envahissantes» (EEE), ce qui signifie qu’ils peuvent être visés par des mesures d’éradication (tirs, piégeage, arrachage, bâchage…). Cependant, «toutes les espèces introduites ne sont pas … "
Quels sont les effets de la crise de la biodiversité sur les maladies infectieuses ? Une étude parue dans la revue Molecular Ecology apporte de nouveaux éléments de réponse à cette interrogation. Les scientifiques ont utilisé des outils moléculaires innovants pour étudier un groupe de maladies zoonotiques transmises par des insectes vecteurs en Amazonie : les leishmanioses. INEE-CNRS, 21.02.2022 "Leurs résultats montrent qu'une altération locale de la diversité de mammifères sauvages a deux conséquences opposées sur la circulation de ces parasites : d'une part, les écosystèmes les plus appauvris sont dominés par des mammifères réservoirs de leishmaniose, ce qui contribue à accroître la transmission. Mais d’autre part, ces écosystèmes contiennent également des populations d'insectes vecteurs moins importantes. La cumulation de ces deux mécanismes induit donc un impact global relativement faible sur le risque d'infection." Référence - Biodiversity and vector-borne diseases: host dilution and vector amplification occur simultaneously for Amazonian leishmaniases. Kocher A, Cornuault J, Gantier JC, Manzi S, Chavy A, Girod R, Dusfour I, Forget PM, Ginouves M, Prévot G, Guégan JF, Bañuls AL, de Thoisy B, Murienne J. Molecular Ecology.
[Image] Contenu d'un piège entomologique observé à la loupe binoculaire. Sous la pince, un phlébotome. Crédit : Arthur Kocher
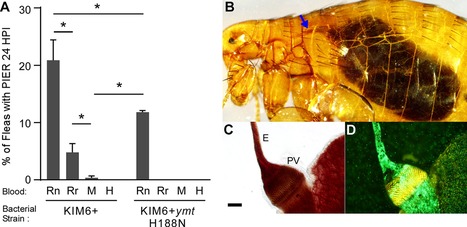
CARTE BLANCHE. L’étude de l’adaptation de « Yersinia pestis » à ses différents hôtes permet de comprendre comment la bactérie responsable de la peste évite les culs-de-sac évolutifs, explique la biologiste Alice Lebreton dans sa carte blanche au « Monde ». Alice Lebreton, 08.12.2021 (abonnés) "Depuis la découverte par Paul-Louis Simond du rôle pivot joué par la puce dans la transmission de la peste, en 1898 à Karachi, cette zoonose est devenue un cas d’école pour l’étude des maladies véhiculées par des insectes. Selon le modèle écologique classiquement retenu, la bactérie responsable de la peste, Yersinia pestis, circule essentiellement entre les animaux qui constituent son réservoir naturel – les rongeurs –, à travers la piqûre par les puces. Ces dernières absorbent le sang infecté puis hébergent les bactéries dans leur tube digestif, et peuvent les transmettre à un nouvel animal en le piquant. Elles sont alors les vecteurs de la maladie, créant des cycles d’infection rongeur-puce-rongeur. Dans ce modèle, l’homme, bien que piqué occasionnellement par des puces infectieuses et lui-même vulnérable à la maladie, reste en général un cul-de-sac pour les transmissions ultérieures ; en effet, les puces de rat n’établissent pas de relations de parasitisme aussi intimes avec l’homme qu’avec les rongeurs sociaux. Afin de mieux cerner les paramètres qui modulent le passage de la bactérie entre réservoirs et vecteurs, un pan des recherches sur la peste vise à identifier les sauts évolutifs qui ont permis l’adaptation de Yersinia pestis à ses différents hôtes. Certains travaux s’attachent ainsi à identifier quels gènes, acquis par la bactérie depuis l’Antiquité, lui ont donné les capacités exceptionnelles de dissémination qui ont conduit aux pandémies de peste, par comparaison avec des génomes de Yersinia isolés de victimes du néolithique ou de l’âge du bronze. L’un de ces gènes, ymt, est supposé améliorer la transmission de la bactérie par les puces ; en effet, ymt n’a pas d’influence sur la virulence de Yersinia chez les animaux réservoirs, mais favorise la colonisation du tube digestif des puces par les bactéries qui le possèdent. Toutefois, l’hypothèse d’un rôle direct de ymt dans l’adaptation aux insectes se heurtait jusqu’ici à une énigme : ymt confère un avantage aux bactéries qui le possèdent lorsque les puces se nourrissent du sang infecté de certaines espèces, comme le rat noir ou la souris (ou même l’homme), mais pas si elles ingurgitent du sang de rat brun. Et, pourtant, ymt ne joue aucun rôle dans la prolifération des bactéries chez l’animal donneur. Un avantage génétique Ce paradoxe apparent a été partiellement résolu par les auteurs d’une étude publiée mi-octobre dans la revue PLOS Pathogens." (...) [Image] Y. pestis Ymt mutant induces PIER in X. cheopis fleas when brown rat blood is used for the infectious blood meal.
... Le rôle de la puce du chat commence à être bien élucidé dans l’épidémiologie de la maladie des griffes du chat et de nouveaux vecteurs potentiels ont été récemment identifiés, qu’il s’agisse des tiques ou des mouches piqueuses. Les connaissances actuelles concernant l’étiologie, les nouvelles manifestations cliniques et l’épidémiologie de ces zoonoses émergentes sont présentées. Communication scientifique Séance du 1er mars 2005
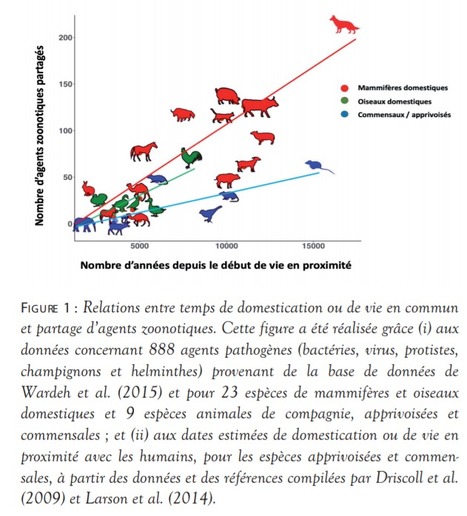
"Nouvelle parution dans @BulletinFrance : "Elevage, biodiversité et émergence de pandémies" par Serge Morand @serge_morand (@Cirad)" Bulletin Académie Vétérinaire France sur Twitter, 21.06.2021
https://twitter.com/BulletinFrance/status/1406855590899597317 Par Serge MORAND RÉSUMÉ "Le présent article a pour objet de résumer les connaissances sur les dynamiques d’émergence et d’épidémies de zoonoses liées. Premièrement, en reconnaissant que le processus de domestication est structurant de l’écologie et de l’épidémiologie des zoonoses passées comme des émergences et épidémies actuelles. Deuxièmement, en montrant comment l’augmentation de l’élevage semble être un facteur essentiel dans les dynamiques épidémiologiques et d’émergences de nouvelles zoonoses. Le lien entre élevage, biodiversité et zoonoses s’explique par le fait que les animaux domestiqués sont des ponts épidémiologiques entre la faune sauvage et les humains. Toute augmentation des densités d’animaux de rente et particulièrement dans des pays hébergeant une forte biodiversité est donc supposée accroître les risques d’émergences et d’épidémies de zoonoses. L’absence d’une bonne compréhension de l’émergence et de la transmission des zoonoses ne doit cependant pas nous empêcher de mieux agir afin de prévenir les risques zoonotiques locaux comme les crises sanitaires globales." CONCLUSION "La prochaine émergence est certaine et pourtant nous ne pouvons pas prédire quel agent, quel réservoir animal, quel lieu géographique, ni quand elle aura lieu. Les systèmes de santé publique et de santé vétérinaire sont donc contraints d’accroître leurs capacités de surveillance comme leurs capacités de résilience en cas d’épidémies ou de pandémies. L’urgence est de s’attaquer aux causes favorisant les émergences des zoonoses et leurs transmissions à large échelle. Pour cela, nous devons admettre la complexité des facteurs en jeu, nécessitant des recherches pluridisciplinaires, et la complexité des actions publiques nécessitant une intersectorialité renouvelée. Cette urgence nécessite également de renforcer le dialogue entre science et décisions politiques." [parasites, arthropodes, vecteurs] Key-Words: domestication, livestock, wildlife, zoonoses, mobility, emerging infectious diseases, epidemics, One Health
|



 Your new post is loading...
Your new post is loading...












![[Rétro] Vers une surveillance précoce des zoonoses virales en milieu forestier tropical grâce aux fourmis légionnaires | EntomoNews | Scoop.it](https://img.scoop.it/NWX2HPG5wJ8L3LSIBlNOSTl72eJkfbmt4t8yenImKBVvK0kTmF0xjctABnaLJIm9)







https://www.scoop.it/topic/les-insectes-ne-parlent-pas-francais/?&tag=zoonoses